实验室必须对高效液相色谱仪进行认证,通常应用4Q模型认证方法。4Q模型通常由四个相关联阶段构成:设计认证(DQ)、安装认证(IQ)、操作认证(OQ)及性能认证(PQ)。
1、全面了解4Q模型
仪器认证生命周期通常被描述或默认为线性模型。要全面了解4Q模型,最好将前三个阶段用V模型表示(如图1)。在此简化的V模型中,更容易看出4Q各阶段之间的关系。OQ证实了USP <1058>(1)中概括出的性能指标。
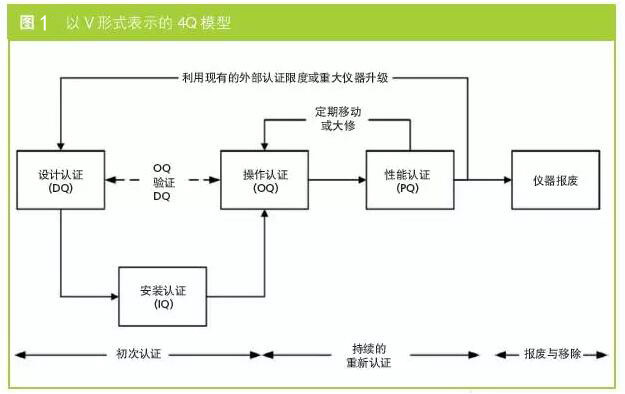
对于DQ的管理具有持续动态需求,例如药典每次更新时仪器的DQ均需进行重新审核。图2强调在仪器进行重要升级或采用以前没有涉及到的新方法时,均需要对DQ进行审查以确保仪器的适用性。如果没有该反馈回路,将会存在仪器无法适用于新应用的风险。该图还着重表明OQ中是否需要包含不同设定点以测试适用范围。OQ能够基本涵盖日常风险,在某确定时间段之后对现有仪器进行重新认证,通常需要预防性维护服务;。OQ用于证明仪器在固定时间点处依据DQ中的性能指标进行操作,从而证明其符合预期用途。
2、对风险评估的理解
首先是4Q模型的角度对高效液相色谱仪(HPLC)的生命周期风险评估进行讨论。第一步便是针对液相色谱在操作认证阶段(OQ阶段)出现的问题进行风险评估。
风险管理与评估已逐渐成为制药行业中的专业术语,对监管机构及制药行业到底意味着什么?从监管机构角度出发,行业必须进行风险评估用以控制某项活动及过程中最关键部分,并努力降低风险,将稀有资源放在最需要的地方,并确定风险管理改进办法。
出现问题的原因有哪些?
首先,从可能使HPLC操作出现问题之处入手(如图2所示)。液相色谱仪由四个模块组成:泵、进样器(自动进样器)、柱温箱及检测器,图中省略了色谱柱。每个模块下方列出可能发生的错误。如果您实验室中的仪器不具备某些特定功能,问题可能会避免,例如等度泵将不会产生梯度错误。
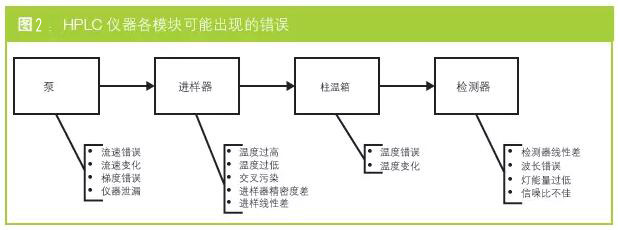
其次,需要考虑这些特定错误可能在OQ或PQ过程中被检测到。其中,PQ分为三个方面:系统适用性测试(SST)、检测问题仪器以及额外SST组,可对SST中涵盖的参数进行测定。
3、仪器性能认证
重点在于仪器生命周期的操作阶段需要考虑PQ。历史上,USP<1058>于2008年首次实施之前采用的是1987年美国食品和药品管理局(FDA)的过程认证指南,并将其应用于分析仪器认证之中,该指南被实验室及服务供应商以不同方式诠释。
OQ和PQ的确具有完全不同的功能。OQ与标准化条件下仪器测试相关。因此,可以相对于DQ确认仪器在实验室中的正确操作,而PQ则针对重复进行OQ仪器在实际使用条件下的适用性。某些实验室可能会在OQ或PQ需要重复进行的条件下做出取舍。任何“新”仪器在用于产生GxP数据之前都必须进行OQ和PQ。
4、OQ与PQ
在仪器生命周期中需要对OQ与PQ的不同角色进行持续支持,实现这一目标有多种选择。验证仪器针对其预期用途的可接受性能(表1)。
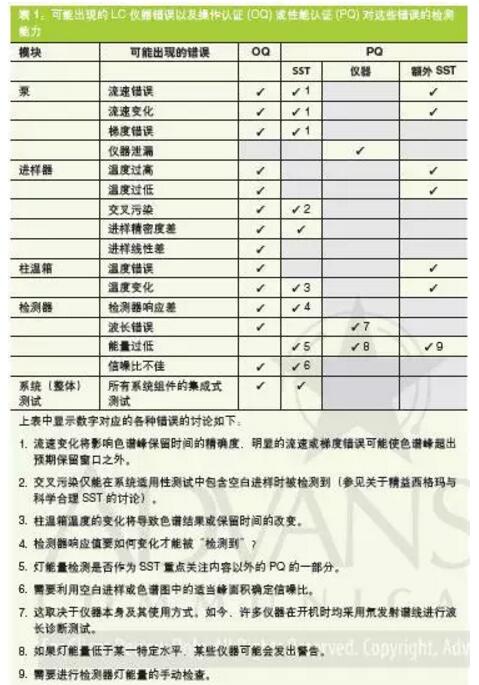
DQ和PQ之间存在直接关系,后者需要证明正在进行的仪器操作与前者的预期用途要求一致。
OQ相对于PQ的不确定性之一在于需要确定仪器生命周期中应该执行性能认证的频率,以及触发认证要求的原因。
在缺乏“黑白指南”的情况下,HPLC系统通常需要每年进行一次重新认证,从而将仪器维护与认证工作联系在一起。这种关联使得用户可能认为仪器在维护过程中修正了以前未能检测到的错误,但也因为这项错误在维护中得到了修正,因此后续认证测试中将不再对其进行评估或检测。
(内容参考实验与分析)










